A systematic review of the effect of immune strategy switching on poliovirus monitoring in the environment
-
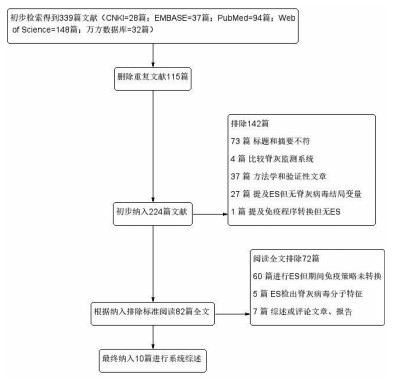
摘要: 本文用系统评价的方法评估脊髓灰质炎免疫策略转换对环境监测脊髓灰质炎病毒设计、检出情况和型别产生的影响,为正在进行免疫策略转换的国家提供参考。利用检索词“环境监测”、“污水”、“脊髓灰质炎病毒”进行在英文数据库PubMed、EMBASE、Web of Science、Cochrance Library和中文数据库CNKI、万方数据知识服务平台检索并筛选、提取文献信息。共纳入10篇在进行环境监测脊髓灰质炎病毒期间进行免疫策略转换的文献,根据不同国家气候和人群免疫状况不同,脊髓灰质炎病毒在污水中的检出率和最后检出时间也有所不同。免疫策略转换期间环境监测的设计存在差异,分离到脊髓灰质炎病毒Ⅱ型和Ⅲ型较多。免疫策略转换前通过外环境检出较多的脊髓灰质炎疫苗相关株,与Sabin疫苗株有99%以上的同源性。在脊髓灰质炎根除的最后阶段,特别是正在进行免疫策略转换的国家,应加强环境监测,为证实脊髓灰质炎消灭提供证据。Abstract: We completed a systematic review to evaluate the impact of polio immunization strategy transformation on the design, detection and type of poliovirus in environmental surveillance, so as to provide reference for countries undergoing polio conversion. We searched PubMed, EMBASE, Web of Science, Cochrane Library, CNKI and Wan-fang database by using the terms "environmental monitoring", "sewage" and "poliovirus". Then we screened and extracted the information for systematic evaluation. A total of 10 articles on immune strategy transformation during environmental surveillance of poliovirus were included. According to the climate and population immune status of different countries, the detection rate and final detection time of poliovirus in sewage were different. There were also differences in the design of environmental monitoring during the transformation period of immunization strategies. Poliovirus types Ⅱ and Ⅲ were major strains. Before the change of immunization strategy, there were more polio vaccine-related strains in the environment, which had more than 99% homology with Sabin vaccine strains. In the final phase of polio eradication, especially in countries undergoing a shift in immunization strategies, environmental monitoring should be strengthened to provide evidence for confirmation of polio eradication.
-
表 1 文献偏倚风险评价
Table 1. Risk assessment of literature bias
评价条目 纳入文献 英国[11] 新西兰[12] 阿根廷[13] 瑞士[14] 墨西哥[15] 印度尼西亚[16] 日本[17] 乌拉圭[18] 喀麦隆[19] 莫斯科[20] 设计科学 是 是 是 是 是 是 是 是 是 是 数据收集策略合理 不清楚 不清 是 是 是 是 不清楚 是 不清楚 不清楚 报告了样本应答率 否 不清楚 是 是 是 是 是 是 是 是 样本对总体的代表性好 是 是 是 是 是 不清楚 是 不清楚 不清楚 不清楚 研究目的和方法合理 是 不清楚 是 是 是 是 是 是 是 是 报告了检验效能 否 否 否 否 否 否 否 否 否 否 统计方法合理 是 是 是 是 是 是 是 是 是 是 总计(分) 4.5 4.5 6.0 6.0 6.0 5.5 5.5 5.5 5.0 5.0 表 2 纳入文献的基本特征
Table 2. Studies included in the review and characteristics of the study
第一作者 发表年份 国家(地区) 免疫策略转换时间(年、月) 采集时间(年、月) 采集方法 采集体积(L) 采集间隔 采集点人口(万) 样品浓缩方法 病毒分离鉴定方法 PV检出率(%) Horstmann et.al[11] 1972 英国 1961(开展Sabin OPV临床试验) 1961-1967 trapb / 1次/周 3.0 两相分离法 细胞培养法 / Huang et.al [12] 2005 新西兰 2002.2 2001.9-2003.4 / / 1次/周 6.5~90.0 / / 94.0 Mueller et.al [13] 2008 阿根廷 2005-2006a 2005.5-2006.4 grabc 1.500 1次/周 5.0~136.0 两相分离法 细胞培养法 56.0 Zurbriggen et.al [14] 2008 瑞士 2001前:主要用OPV;2001-2004:IPV-OPV;2004:IPV-only 2004.1-2006.10 grab 0.500 1次/周 5.5~34.0 SiO2沉淀法和两相分离法 细胞培养法;ELISA、RT-PCR型内鉴定 11.5 Esteves-Jaramillo et.al[15] 2014 墨西哥 2007(OPV-only转为IPV- OPV);2010.5 (OPV扩大免疫) 2010.5 grab 1.000 2次/周~ 1次/两周 / 两相分离法 细胞培养法 54.0 Wahjuhono et.al [16] 2014 印度尼西亚 2007.9 2004.7-2012.12 grab 1.000 1次/周~ 2次/周 / 两相分离法 细胞培养法 23.0 Nakamura et.al [17] 2015 日本 2012.9 2010.4-2013.1 1.000 1次/月 18.0~19.0 阴离子膜吸附法 细胞培养法 18.6 Lizasoain et.al [18] 2018 乌拉圭 2012.5 2011.3-2013.4 grab 0.042 2次/周~ 2次/月 / 阴离子膜吸附-洗脱 PCR和细胞培养法 0.0 Njile et.al [19] 2019 喀麦隆 2016.4 2016.1-2017.12 / 1.000 2次/周 / 两相分离法 细胞培养法 7.2 Ivanova et.al [20] 2019 莫斯科 2016.4 2004-2017 trap / 1次/周 100.0~600.0 两相分离法 细胞培养法、型内鉴定:ELISA、RT-PCR、实时定量RT-PCR 42.7 注:a:2005年5-8月(IPV),2005年8-9月(OPV),2005年9-12月(IPV),2006年1-4月(OPV);trapb:通过在污水中悬挂一个含非特异性吸附材料的袋子≥1天后将其取出并运送至实验室进行洗脱;grabc:在选定的样品采集点采集一定数量的未处理过的污水样品。 表 3 免疫策略转换下环境监测PV设计的改变
Table 3. Changes in the design of environmental monitoring PV under the change of immunization strategy
表 4 环境监测PV的遗传学特征
Table 4. The genetic characteristics of environmental monitoring PV
国家 VP1序列测定 核苷酸突变型别(突变个数/突变频率) 遗传特征改变时期 日本 均为SL SL3a(6) 免疫策略转换前 新西兰 均为SL OPV/IPV转换6、9、12个月后 印度尼西亚 均为SL SL2b(≥6)、SL1c(≥10)、SL3(≥10) 84%的SL为转换前 阿根廷 均为SL 77%的SL(≥1)、3%的SL(≥5) 免疫策略转换前、中、后 喀麦隆 均为SL SL2(≤2) SL2:免疫策略转换前 墨西哥 SL和VDPV VDPV1(12-13)、VDPV2(6-7) SL3:扩大免疫1周后VDPV2:扩大免疫前和疫中VDPV1:扩大免疫后19周 莫斯科 SL和VDPV VDPV2(17.6%) VDPV2:免疫策略转换前 瑞士 均为SL 免疫策略转换后 注:SL3a:Sabin-like poliovirus Ⅲ;SL2b:Sabin-like poliovirus Ⅱ; SL1c:Sabin-like poliovirus Ⅰ。 -
[1] Menant JC, Gandevia SC. Poliomyelitis [J]. Handb Clin Neurol, 2018, 159:337-344. DOI: 10.1016/b978-0-444-63916-5.00021-5. [2] Kroiss SJ, Ahmadzai M, Ahmed J, et al. Assessing the sensitivity of the polio environmental surveillance system [J]. Plos One, 2018, 13(12). DOI: 10.1371/journal.pone.0208336. [3] OReilly KM, Verity R, Durry E, et al. Population sensitivity of acute flaccid paralysis and environmental surveillance for serotype 1 poliovirus in Pakistan: an observational study [J]. BMC Infect Dis, 2018, 18(1):176. DOI: 10.1186/s12879-018-3070-4. [4] Garg A, Pattamadilok S, Bahl S. Successes and challenges of expansion of environmental poliovirus surveillance in the WHO South-East Asia Region [J]. WHO South East Asia J Public Health, 2018, 7(2):122-128. DOI: 10.4103/2224-3151.239424. [5] Li L, Ivanova O, Driss N, et al. Poliovirus excretion among persons with primary immune deficiency disorders: summary of a seven-country study series [J]. J Infect Dis, 2014, 210(Suppl 1):S368-S372. DOI: 10.1093/infdis/jiu065. [6] Benschop KSM, van der Avoort HG, Jusic E, et al. Polio and measles down the drain: environmental enterovirus surveillance in the Netherlands, 2005 to 2015 [J]. Appl Environ Microbiol, 2017, 83(13). DOI: 10.1128/AEM.00558-17. [7] Alam MM, Shaukat S, Sharif S, et al. Detection of multiple cocirculating wild poliovirus type 1 lineages through environmental surveillance: impact and progress during 2011—2013 in Pakistan [J]. J Infect Dis, 2014, 210Suppl 1:324-332. DOI: 10.1093/infdis/jiu160. [8] Brouwer AF, Eisenberg JNS, Pomeroy CD, et al. Epidemiology of the silent polio outbreak in Rahat, Israel, based on modeling of environmental surveillance data [J]. Proc Natl Acad Sci USA, 2018, 115(45):E10625-E10633. DOI: 10.1073/pnas.1808798115. [9] Chen P, Liu Y, Wang H, et al. Environmental surveillance complements case-based surveillance of acute flaccid paralysis in polio endgame strategy 2019-2023 [J]. Appl Environ Microbiol, 2020, 86(15). DOI: 10.1128/aem.00702-20. [10] Hovi T, Shulman LM, van der Avoort H, et al. Role of environmental poliovirus surveillance in global polio eradication and beyond [J]. Epidemiol Infect, 2012, 140(1):1-13. DOI: 10.1017/s095026881000316x. [11] Horstmann DM, Emmons J, Gimpel L, et al. Enterovirus surveillance following a community-wide oral poliovirus vaccination program-7 year study [J]. Epidemiol Rev, 1973, 97(3):173-186. DOI: 10.1093/oxfordjournals.aje.a121498. [12] Huang QS, Greening G, Baker MG, et al. Persistence of oral polio vaccine virus after its removal from the immunisation schedule in New Zealand [J]. Lancet, 2005, 366(9483):394-396. DOI: 10.1016/s0140-6736(05)66386-6. [13] Mueller JE, Bessaud M, Huang QS, et al. Environmental poliovirus surveillance during oral poliovirus vaccine and inactivated poliovirus vaccine use in Cordoba Province, Argentina [J]. Appl Environ Microbiol, 2009, 75(5):1395-1401. DOI: 10.1128/aem.02201-08. [14] Zurbriggen S, Tobler K, Abril C, et al. Isolation of sabin-like polioviruses from wastewater in a country using inactivated polio vaccine [J]. Appl Environ Microbiol, 2008, 74(18):5608-5614. DOI: 10.1128/aem.02764-07. [15] Esteves-Jaramillo A, Estivariz CF, Pearanda S, et al. Detection of vaccine-derived polioviruses in Mexico using environmental surveillance [J]. J Infect Dis, 2014, 210:S315-S323. DOI: 10.1093/infdis/jiu183. [16] Wahjuhono G, Revolusiana, Widhiastuti D, et al. Switch from oral to inactivated poliovirus vaccine in Yogyakarta Province, Indonesia: summary of coverage, immunity, and environmental surveillance [J]. J Infect Dis, 2014, 210:S347-S352. DOI: 10.1093/infdis/jiu060. [17] Nakamura T, Hamasaki M, Yoshitomi H, et al. Environmental surveillance of poliovirus in sewage water around the introduction period for inactivated polio vaccine in Japan [J]. Appl Environ Microbiol, 2015, 81(5):1859-1864. DOI: 10.1128/aem.03575-14. [18] Lizasoain A, Burlandy FM, Victoria M, et al. An environmental surveillance in uruguay reveals the presence of highly divergent types of human enterovirus species C and a high frequency of species A and B types [J]. Food Environ Virol, 2018, 10(4):343-352. DOI: 10.1007/s12560-018-9351-7. [19] Njile DK, Sadeuh-Mba SA, Endegue-Zanga MC, et al. Detection and characterization of polioviruses originating from urban sewage in Yaounde and Douala, Cameroon 2016-2017 [J]. BMC Res Notes, 2019, 12(1):248. DOI: 10.1186/s13104-019-4280-6. [20] Ivanova OE, Yarmolskaya MS, Eremeeva TP, et al. Environmental surveillance for poliovirus and other enteroviruses: Long-Term Experience in Moscow, Russian Federation, 2004-2017 [J]. Viruses, 2019, 11(5). DOI: 10.3390/v11050424. [21] Duintjer Tebbens RJ, Zimmermann M, Pallansch MA, et al. Insights from a systematic search for information on designs, costs, and effectiveness of poliovirus environmental surveillance systems [J]. Food Environ Virol, 2017, 9(4):361-382. DOI: 10.1007/s12560-017-9314-4. [22] Kew O, Pallansch M. Breaking the last chains of poliovirus transmission: progress and challenges in Global Polio Eradication [J]. Annu Rev Virol, 2018, 5(1):427-451. DOI: 10.1146/annurev-virology-101416-041749. [23] Greene SA, Ahmed J, Datta SD, et al. Progress toward polio eradication - worldwide, January 2017-March 2019 [J]. MMWR Morb Mortal Wkly Rep, 2019, 68(20):458-462. DOI: 10.15585/mmwr.mm6820a3. [24] Duintjer Tebbens RJ, Thompson KM. Polio endgame risks and the possibility of restarting the use of oral poliovirus vaccine [J]. Expert Rev Vaccines, 2018, 17(8):739-751. DOI: 10.1080/14760584.2018.1506333. [25] Alleman MM, Jorba J, Greene SA, et al. Update on vaccine-derived poliovirus outbreaks-worldwide, July 2019-February 2020 [J]. MMWR Morb Mortal Wkly Rep, 2020, 69(16):489-495. DOI: 10.15585/mmwr.mm6916a1. [26] Altamirano J, Sarnquist C, Behl R, et al. OPV vaccination and shedding patterns in Mexican and US children [J]. Clin Infect Dis, 2018, 67(suppl_1):S85-S89. DOI: 10.1093/cid/ciy636. [27] Asghar H, Diop OM, Weldegebriel G, et al. Environmental surveillance for polioviruses in the Global Polio Eradication Initiative [J]. J Infect Dis, 2014, 210(Suppl1):S294-S303. DOI: 10.1093/infdis/jiu384. [28] Diop OM, Asghar H, Gavrilin E, et al. Virologic monitoring of poliovirus type 2 after oral poliovirus vaccine Type 2 withdrawal in april 2016-worldwide, 2016-2017 [J]. MMWR Morb Mortal Wkly Rep, 2017, 66(20):538-542. DOI: 10.15585/mmwr.mm6620a4. -




 下载:
下载: